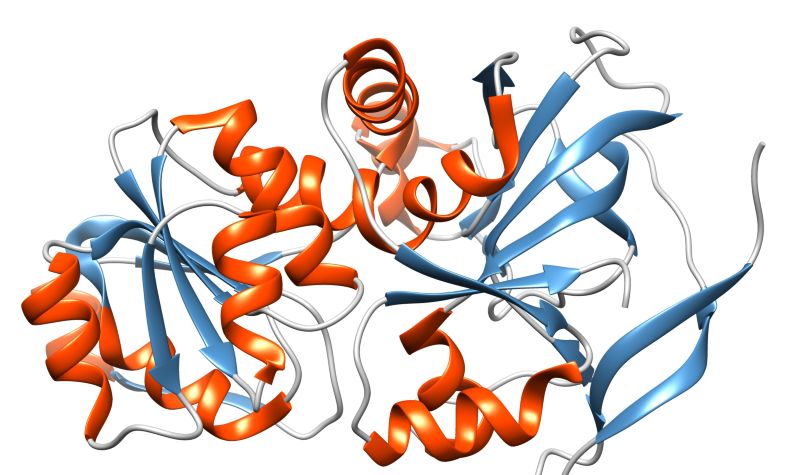
Die Technologieplattform BIOExpresSPro stellt Werkzeuge für die Identifizierung und Produktion industrierelevanter Enzyme bereit, die beispielsweise Pflanzenbiomasse effektiv abbauen können. Mithilfe innovativer Biosensoren auf Basis von Fluoreszenzproteinen können im Projekt nun Sekretionsprozesse direkt verfolgt werden. Ein automatisiertes Mini-Pilotanlagen-Mikrobioreaktorsystem mit höherem Kultivierungsdurchsatz wurde zudem validiert und steht nun für das Stammscreening bereit.
Ein wichtiger Teil der Bioökonomie ist die Erschließung und Nutzung biologischer Ressourcen, um daraus nachhaltige, biobasierte Produkte herzustellen. Pflanzen nehmen hier eine Schlüsselstellung ein, da sie aus Wasser, Kohlenstoffdioxid und Sonnenlicht Biomasse erzeugen. Sie stellen daher einen nahezu unerschöpflichen Rohstoffvorrat für die bioökonomische Verwertung und industrielle Wertschöpfung dar. Um diese pflanzlichen Rohstoffe jedoch nachhaltig nutzen zu können, müssen sie zunächst zugänglich gemacht werden. Eine Strategie, diesen Zugang unter umweltfreundlichen Bedingungen zu erhalten, ist der Einsatz von Enzymen.
Hidden champions
Enzyme sind Biokatalysatoren, die biochemische Reaktionen beschleunigen. Dabei arbeiten Enzyme sehr effizient. Ein Enzym katalysiert eine chemische oder biochemische Reaktion, indem es ein bestimmtes Ausgangsmolekül, das Substrat, in ein Produkt umwandelt und dabei selbst unverändert aus der Reaktion wieder hervorgeht. Enzyme sind also die „hidden champions“, die „Arbeitspferde“ der industriellen Biotechnologie. Sie werden unter anderem als Helfer in der Nahrungsmittel- und Futtermittelindustrie eingesetzt, aber auch in der Kosmetik-, Textil-, Papier- und Zellstoffindustrie, der chemischen Industrie, bei der Gewinnung von Kraftstoffen, in der Agrarindustrie sowie in der medizinischen und pharmazeutischen Industrie.
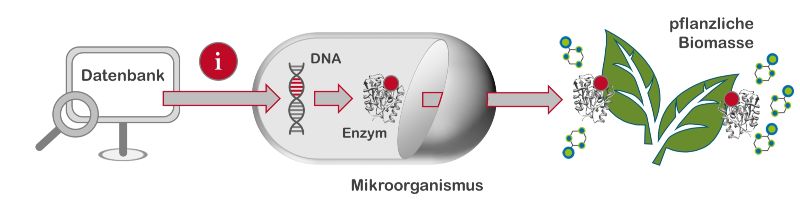
Ziel des hier vorgestellten BioSC Boost-Fund-Projektes „BIOExpresSPro“ war es, in einem ersten Schritt natürlich vorkommende Enzyme zu identifizieren, die pflanzliche Biomasse abbauen können. Solche Enzyme kommen beispielsweise in Pilzen und Bakterien vor, die in der Natur für das Verrotten von Laub bis hin zu ganzen Baumstämmen sorgen. Oftmals sind diese in der Natur beheimateten Mikroorganismen aber nicht für den Einsatz im Labor geeignet. Ihre Ansprüche an die Umgebung, wie Nährstoffangebot oder Temperatur, sind meist zu komplex. Daher war es das zweite Ziel, die Gene, mit denen diese spezialisierten Enzyme hergestellt werden können, in gut handhabbare Labor-Mikroorganismen zu übertragen, die dann die gewünschten Enzyme produzieren und ausscheiden. In einem weiteren Schritt sollten die gewünschten Enzyme optimiert werden. Um diese Ziele zu erreichen, war die breite Expertise aus Biologie, Biochemie, Biotechnologie, Bioprozesstechnik, Bioanalytik sowie Bioinformatik gefragt. Darüber hinaus wurde „BIOExpresSPro“ während der gesamten Projektlaufzeit von zwei assoziierten Industriepartnern beraten. Bei diesen Partnern handelte es sich um das Unternehmen AB Enzymes GmbH und die evocatal GmbH, die inzwischen als evoxx technologies GmbH von Advanced Enzyme Technologies Ltd. übernommen wurde.
Fachwissen bündeln
„BIOExpresSPro“ bündelt als Technologieplattform dieses weit verzweigte Fach- und Industriewissen in sogenannten Pipelines. So wurde zunächst eine Vorhersage-Pipeline zur Identifizierung neuer biomasseabbauender Enzyme etabliert. Hier wurden mithilfe ausgeklügelter Algorithmen öffentlich zugängliche Datenbanken wie BRENDA und UniProt bioinformatisch durchsucht. Dadurch konnten bisher unbekannte Enzyme gefunden werden, deren Eigenschaften auch bei den Industriepartnern sehr begehrt sind. Derartige Enzyme wurden so zum Beispiel in den Bakteriengattungen Arthrobacter und Pseudomonas entdeckt. Um solche Enzyme in bioökonomischen Prozessen einsetzen zu können, müssen sie in ausreichenden Mengen produziert werden. Dazu wurden die Gene der bioinformatisch identifizierten projektrelevanten Enzyme in einer weiteren Pipeline mithilfe modernster Klonierungs-Methoden in gut handhabbare mikrobielle Wirte eingeschleust, welche die gesuchten Enzyme dann in großen Mengen synthetisierten. Durch die gezielte Evolution der Wirtszellen sorgten die Wissenschaftler zudem dafür, dass die gewünschten Enzyme in größeren Mengen aus den Wirtszellen heraus geschleust werden und nicht etwa im Zellinneren verbleiben. Diese sogenannte Sekretion erleichtert die spätere Ernte der Enzyme ungemein.
Um die Machbarkeit des Verfahrens zu belegen, wurde zunächst eine umfangreiche genetische Bibliothek des Enzyms Cutinase aus dem Pilz Fusarium solani pisi generiert und in Wirtsorganismen zum Einsatz gebracht. Cutinasen sind in der Lage, den wächsernen Schutzpanzer von Pflanzen zu knacken. Sie öffnen somit die Pforten in das Innere der Pflanzen und machen sie für weitere Abbauprozesse zugänglich. Für die industrielle Verwertung von Pflanzenbiomasse spielen diese Enzyme daher eine entscheidende Rolle. In einem nächsten Schritt gelang es, die Cutinase-Produktion in den in der Biotechnologie weit verbreiteten Bakterien Escherichia coli und Corynebacterium glutamicum zu optimieren.
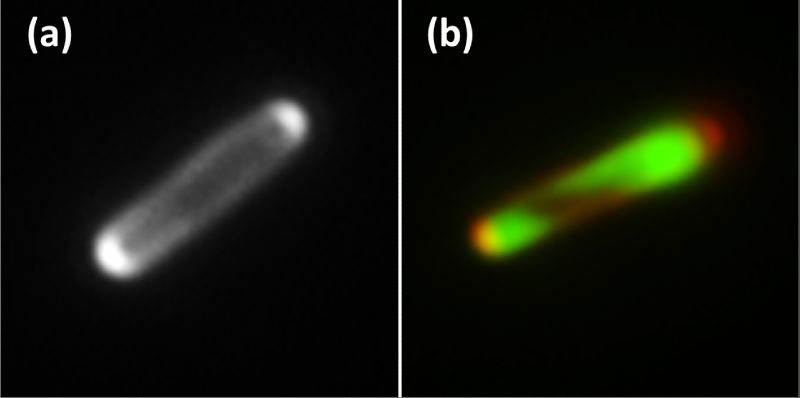
Erfolgreich Enzyme produzieren
Darüber hinaus wurden für die Technologieplattform BIOExpresSPro auch neuartige Biosensoren entwickelt, mit denen die Sekretion des synthetisierten Wunschenzyms aus den Zellen konzentrations- und ortsabhängig direkt beobachtet werden kann. Das Verfahren beruht auf einem Fluoreszenzprotein, das Zellen, die besonders stark sekretieren, aufleuchten lässt. Mithilfe dieser Technik gelang es, eine neue Hypersekretionsmutante von C. glutamicum zu isolieren, die im Vergleich zum Wildtyp-Stamm signifikant höhere Mengen des gewünschten Enzyms ins Medium ausscheidet. Parallel dazu wurde ein weiterer neuartiger Fluoreszenz-Biosensor etabliert, der zur Analyse von Sekretion und Proteinlokalisierung in E. coli dient. Dieser Biosensor ist in der Lage, das ausgewählte Zielprotein, also zum Beispiel das gewünschte Enzym, aufgrund der Fluoreszenz in der Zelle zu lokalisieren. Da dieser Biosensor innerhalb der Zellen eine andere Fluoreszenzfarbe hat als außerhalb, kann mit seiner Hilfe die Sekretionsrate des gewünschten Enzyms über die innere Zellmembran bestimmt werden. Auf der Ebene der Prozessentwicklung wurde zudem ein automatisiertes Mini-Pilotanlagen-Mikrobioreaktorsystem entwickelt und validiert. Dieses Bioreaktorsystem hilft dabei, in kurzer Zeit Bakterienstämme mit den gewünschten Eigenschaften zu finden, zu isolieren und zu vermehren. Die erzielten Ergebnisse und die im Rahmen von „BIOExpresSPro“ neu entwickelten Technologien waren nach Abschluss der Projektförderung so erfolgversprechend, dass sie in weiterführende Projekte eingeflossen sind, die sowohl vom Bund als auch vom Land NRW und der EU finanziert wurden und werden.
Projektleiter
Dr. Achim Heck
Institut für Molekulare Enzymtechnologie, HHU Düsseldorf
Email
Beteiligte Core Groups
Prof. Dr. Karl-Erich Jaeger, Dr. Achim Heck, Dr. Thomas Drepper, Dr. Katrin Troost, Andreas Woop
Institut für Molekulare Enzymtechnologie, HHU Düsseldorf
Prof. Dr. Michael Bott, Prof. Dr. Roland Freudl, Sarah-Kristin Jurischka
IBG-1 Biotechnologie, Forschungszentrum Jülich
Prof. Dr. Wolfgang Wiechert, Prof. Dr. Marco Oldiges, Dr. Jannick Kappelmann, Dr. Johannes Hemmerich
IBG-1 Biotechnologie, Forschungszentrum Jülich
Prof. Dr. Björn Usadel, Dr. Alexander Vogel
IBG-4 Bioinformatik, Forschungszentrum Jülich
Prof. Dr. Ulrich Schwaneberg, Dr. Anna Joëlle Ruff, Dr. Wei Long
ABBt – Biotechnologie, RWTH Aachen
Industry partners (associated partners)
Dr. Christian Degering, Dr. Michael Puls, Dr. Christian Leggewie
evocatal GmbH, Düsseldorf (currently: evoxx technologies)
Dr. Jari Vehmaanperä, Prof. Dr. Karl-Heinz Maurer
AB Enzymes GmbH, Darmstadt
Projektlaufzeit
1.1.2014 – 31.12.2016
Förderung
BioExpresSPro ist Teil des NRW-Strategieprojekt BioSC und gefördert vom Ministerium für Kultur und Wissenschaft des Landes Nordrhein-Westfalen.
Publikationen
Freier, L, Hemmerich, J, Schöler, K, Wiechert, W, Oldiges, M and von Lieres, E (2016). Framework for kriging-based iterative experimental analysis and design: Optimization of secretory protein production in corynebacterium glutamicum. Engineering in Life Sciences 16(6): 538-549.
Heck, A and Drepper, T (2017). Engineering photosynthetic α-proteobacteria for the production of recombinant proteins and terpenoids. Modern topics in the phototrophic prokaryotes: Environmental and applied aspects. Hallenbeck, P.C. Cham, Springer International Publishing: 395-425.
Hemmerich, J, Rohe, P, Kleine, B, Jurischka, S, Wiechert, W, Freudl, R and Oldiges, M (2016). Use of a sec signal peptide library from bacillus subtilis for the optimization of cutinase secretion in corynebacterium glutamicum. Microbial Cell Factories 15(1): 208.
Loehrer, M, Vogel, A, Huettel, B, Reinhardt, R, Benes, V, Duplessis, S, Usadel, B and Schaffrath, U (2014). On the current status of phakopsora pachyrhizi genome sequencing. Front Plant Sci 5: 377.
MacKellar, D, Lieber, L, Norman, JS, Bolger, A, Tobin, C, Murray, JW, Oksaksin, M, Chang, RL, Ford, TJ, Nguyen, PQ, Woodward, J, Permingeat, HR, Joshi, NS, Silver, PA, Usadel, B, Rutherford, AW, Friesen, ML and Prell, J (2016). Streptomyces thermoautotrophicus does not fix nitrogen. Scientific Reports 6: 20086.
Torra, J, Burgos-Caminal, A, Endres, S, Wingen, M, Drepper, T, Gensch, T, Ruiz-Gonzalez, R and Nonell, S (2015). Singlet oxygen photosensitisation by the fluorescent protein pp2fbfp l30m, a novel derivative of pseudomonas putida flavin-binding pp2fbfp. Photochem Photobiol Sci 14(2): 280-287.