Bio- und Chemotransformationen zu Metaraminol und Tetrahydroisoquinolinen
Metaraminol ist ein pharmazeutischer Wirkstoff, der zur Behandlung von zu niedrigem Blutdruck ein gesetzt wird und dient gleichzeitig als chirale Vorstufe von komplexeren bioaktiven Verbindungen wie den THIQs. Im Rahmen von HyImPAct konnten für alle Kaskadenschritte geeignete Bio-Katalysatoren mit hoher Aktivität gewonnen werden, insbesondere auch für die Umsetzung von realen Substraten aus zellfreien Überständen der vorgeschalteten mikrobiellen Bio-Transformation (Abb.1).
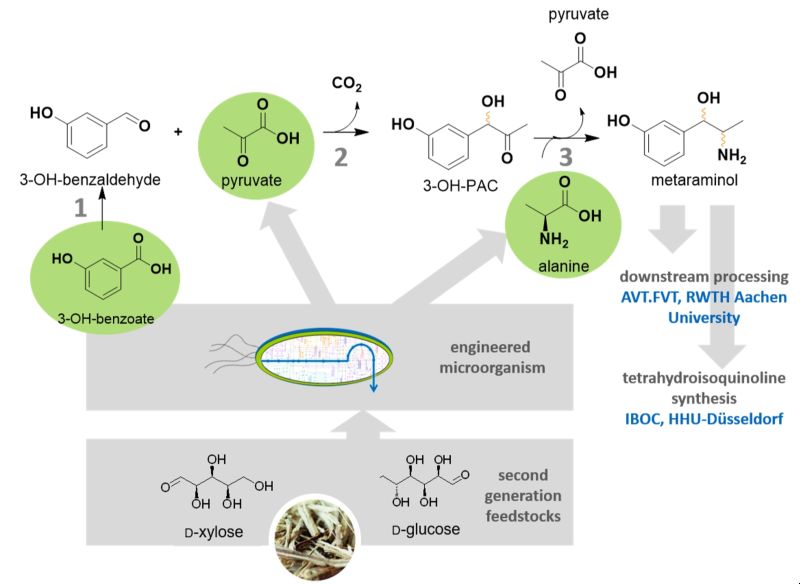
Zunächst werden mithilfe einer dreistufigen enzymatischen Kaskade die verschiedenen biobasierten Vorstufen 3-Hydroxybenzoat, Pyruvat und Alanin in Metaraminol umgesetzt: Ausgehend von 3-Hydroxybenzoat erzeugt eine Carboxylat-Reduktase (CAR (1)) das aromatische Aldehyd 3-Hydroxy-Benzaldehyd, welches anschließend mit Pyruvat durch eine Pyruvatdecarbocylase (PDC (2)) zu einem Hydroxyketon (3-Hydoxy-PAC) ligiert wird. Danach setzt eine Transaminase (TA(3)) das Hydroxyketon unter Verwendung von Alanin als Amindonor zu Metaraminol um.
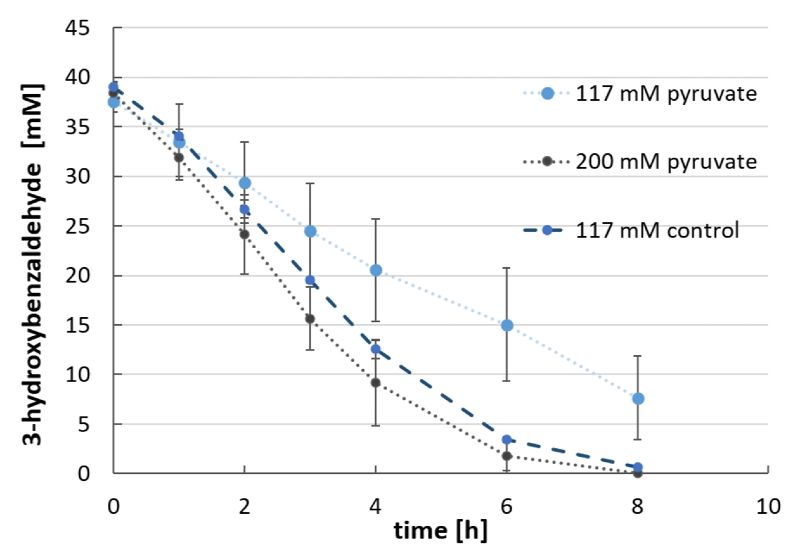
Der erste Schritt der Kaskade konnte durch ein Konzept zur in-vitro Regeneration der verwendeten Cofaktoren effizienter gestaltet werden. Die im zweiten Reaktionsschritt verwendete PDC demonstrierte eine hohe Aktivität und Stereoselektivität in den eingesetzten zellfreien Überständen und ermöglicht so die vollständige Umsetzung von 40 mM 3-Hydroxybenzaldehyd in nur acht Stunden bei einer sehr guten Stereoselektivität von über 94 % ee (Enantiomerenüberschuss).
Eine größere Herausforderung ergibt sich allerdings für dem dritten Kaskadenschritt, bei dem Alanin als biobasiertes Co-Substrat dient. Hier wird eine Transaminase eingesetzt, die Alanin als grüne Alternative zu sonst toxischen und erdölbasierten Amin-Donatoren verwendet und die gezielte Aminierung mit hoher Stereoselektivität erreicht.
Typischerweise erfolgt die Isolation von Alanin aus Kulturüberständen durch Kristallisation. Um Kristalle von hoher Reinheit zu gewinnen, muss zunächst ein breites Spektrum an verschiedenen Verunreinigungen aus der Fermentation abgetrennt werden. Dazu wird typischerweise ein Chromatographie-Schritt durchgeführt.
Für eine detaillierte Analyse der Ausbeuten und der Wirtschaftlichkeit wurden die verschiedenen Kombinationen aus Chromatographie und Kristallisationen in Kombination mit unterschiedlichen Konzentrationen evaluiert. Final wurde eine Kationenaustauschchromatographie in Kombination mit Coolingcrystalization als DSP gewählt, da dieser Aufbau über alle Produkttiter hinweg die geringsten Betriebskosten pro Gramm Produkt aufweist. Es zeigte sich auch, dass für alle untersuchten Varianten die Alaninausbeute bei höherer Ausgangskonzentration steigt, da die Gesamtmenge an verlorenem Produkt innerhalb eines Prozessdesigns nahezu konstant bleibt. Dies führt zu deutlich geringeren spezifischen DSP-Kosten für höhere Alanintiter. Die resultierenden Kristalle können anschließend für die Biokatalyse von Metaraminol eingesetzt werden.

Die resultierende biokatalytische Reaktion arbeitet in diesem Fall sehr nah am thermodynamischen Gleichgewicht, was ohne technische Hilfsmaßnahmen zu niedrigen Ausbeuten im Bereich von 15-20 % Metaraminol führt. Zur Steigerung des Reaktionsumsatzes wurde deshalb ein In-situ-Produkt-Abtrennungsverfahren (ISPR) in Zusammenarbeit mit dem Lehrstuhl für Fluidverfahrenstechnik der RWTH Aachen entwickelt. Das Konzept ermöglicht mittels zweier verschiedener auf Flüssig-Flüssig-Extraktionen eine erhöhte Metaraminol-Ausbeute und minimiert Abfallströme, da die Produktion und ein erster Aufarbeitungsschritt von Metaraminol in einem gemeinsamen Prozess realisiert werden konnten.Zusätzlich wurde ein umfassendes organisches Lösungsmittel-Screening mit der eingesetzten Transaminase durchgeführt, dass eine uneingeschränkte Enzymaktivität und Stabilität in Gegenwart der gewählten organischen Extraktionsphase zeigte.
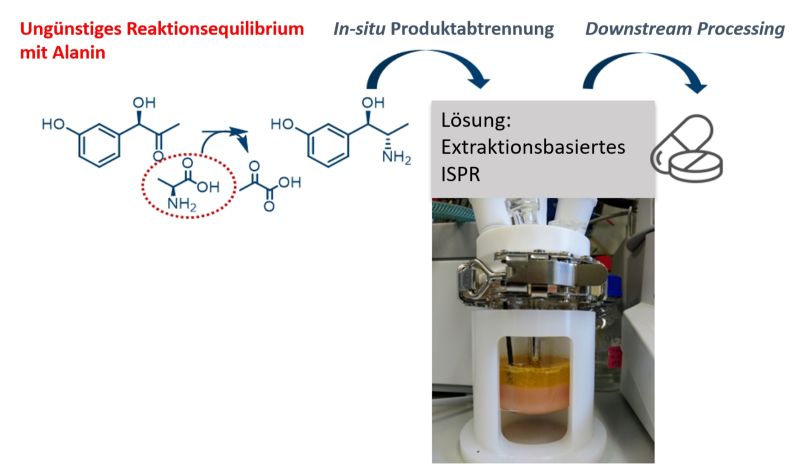
In Kombination mit einer optimierten Isolation des Alanins aus Substratüberständen erhöht sich die Gesamtausbeute an Metaraminol, was wesentlich zur Leistungsfähigkeit des gesamten Hybridprozesses beiträgt. Darüber hinaus wurde eine effiziente Produktrückgewinnung durch Re-Extraktion erreicht, wodurch zusätzliche Prozessschritte und Abfallströme minimiert werden, während das Nebenprodukt Pyruvat für das Recycling innerhalb der Enzymkaskade erhalten bleibt
In einem finalen Schritt kann Metaraminol in eine breite Produktpalette von THIQs umgewandelt werden. Hierfür wurden chemische Syntheseansätze auf Basis der Pictet-Spengler-Reaktion entwickelt und für die Anwendung von biobasiertem Metaraminol als Substrat optimiert.
Prof. Jörg Pietruszka
Andreas Sebastian Klein
Anna Christina Alberecht
Bioorganic Chemistry
HHU Düsseldorf
Prof. Wolfgang Wiechert
Dr.-Ing. Stephan Noack
Prof. Dörthe Rother
Mohamed Labib
Christian Brüsseler
Laura Grabowski
Kevon Mack
Douglas Weber
Jochem Gätgens
IBG-1 Biotechnology
Forschungszentrum Jülich
Prof. Andreas Jupke
Moritz Doeker
Christian Kocks
Thomas Fuchs
AVT - Fluid Processing
RWTH Aachen University
Prof. Michael Bott
Prof. Jan Marienhagen
IBG-1 Biotechnology
Forschungszentrum Jülich